Sodio
Si desea modificar el contenido del articulo debe tener un Corrector Ortográfico instalado en Mozilla Firefox sino haga clic en Instalar Diccionario Español Venezuela
- Visualizando: Tutoriales
 Imprimir contenido
Imprimir contenido
 Proponer un mejor articulo
Proponer un mejor articulo
 Favoritos
Favoritos
- Artículos Relacionados...
Sodio
El sodio es un elemento químico de símbolo Na (del latín, natrium y de árabe natrun) número atómico 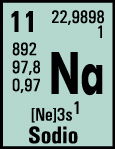 11, fue descubierto por Sir Humphry Davy. Es un metal alcalino blando, untuoso, de color plateado, muy abundante en la naturaleza, encontrándose en la sal marina y el mineral halita. Es muy reactivo, arde con llama amarilla, se oxida en presencia de oxigeno y reacciona violentamente con el agua. El sodio está presente en grandes cantidades en el océano en forma iónica. También es un componente de muchos minerales y un elemento esencial para la vida.
11, fue descubierto por Sir Humphry Davy. Es un metal alcalino blando, untuoso, de color plateado, muy abundante en la naturaleza, encontrándose en la sal marina y el mineral halita. Es muy reactivo, arde con llama amarilla, se oxida en presencia de oxigeno y reacciona violentamente con el agua. El sodio está presente en grandes cantidades en el océano en forma iónica. También es un componente de muchos minerales y un elemento esencial para la vida.
Características principales
Al igual que otros metales alcalinos el sodio es un metal blando, ligero y de color plateado que no se encuentra libre en la naturaleza. El sodio flota en el agua descomponiéndola, desprendiendo hidrógeno y formando un hidróxido. En las condiciones apropiadas reacciona espontáneamente en el agua. Normalmente no arde en contacto con el aire por debajo de 40 °C.
Aplicación del sodio
El sodio metálico se emplea en síntesis orgánica como agente reductor. Es además componente del cloruro de sodio necesario para la vida. Otros usos son:
- En aleaciones antifricción (oro).
- En la fabricación de desodorantes (en combinación con ácidos grasos).
- En la purificación de metales fundidos.
- La aleación Na K, es un material empleado para la transferencia de calor además de desecante para disolventes orgánicos y como reductor. A temperatura ambiente es líquida. El sodio también se emplea como refrigerante.
- Aleado con plomo se emplea en la fabricación de aditivos detonantes para las gasolinas.
- Se emplea también en la fabricación de células fotoeléctricas.
- Iluminación mediante lámparas de vapor de sodio.
- Los óxidos NaO2 generados por combustión controlada con oxígeno se utilizan para intercambiar el dióxido de carbono por oxígeno y regenerar así el aire en espacios cerrados (p. ej. en submarinos)
Abundancia
El sodio es relativamente abundante en las estrellas, detectándose su presencia a través de la línea D del espectro solar, situada aproximadamente en el amarillo. La corteza terrestre contiene aproximadamente un 2,6% de sodio, lo que lo convierte en el cuarto elemento más abundante, y el más abundante de los metales alcalinos. Actualmente se obtiene por electrólisis de cloruro sódico fundido, procedimiento más económico que el anteriormente usado, la electrólisis del hidróxido de sodio. Es el metal alcalino más barato. El compuesto más abundante de sodio es el cloruro sódico o sal común, aunque también se encuentra presente en diversos minerales como halita y zeolitas, etc.
Compuestos
Los compuestos de sodio de mayor importancia industrial son:
-
Sal común (NaCl).
-
Carbonato de sodio (Na2CO3).
-
Bicarbonato de sodio (NaHCO3).
-
Sosa cáustica (NaOH). El hidróxido de sodio, más conocido como sosa cáustica, es una base muy fuerte y corrosiva usada en productos destinados a la limpieza de desagües y al desengrase de hornos. Cuando se disuelve en agua produce una reacción muy exotérmica (-42,9 kJ/mol). Su poder corrosivo hace de la soda cáustica un compuesto letal para los tejidos vivos y los compuestos orgánicos, e incluso puede atacar al vidrio en caso de que el contacto sea permanente. En presencia del dióxido de carbono atmosférico produce carbonato de sodio, por lo que sus soluciones son poco estables.
-
Nitrato de sodio (NaNO3).
-
Tiosulfato de sodio (Na2S2O3 · 5H2O).
-
Bórax (Na2B4O7 · 10H2O).
-
Yoduro de sodio (NaI)
-
Eritorbato de sodio (C6H7NaO6) utilizado en carnes de todo tipo y bebidas no alcohólicas como preservante. Mútageno para el ser humano y letal para algunos ecosistemas acuáticos. leer más...
-
Tripolifosfato de sodio (Na5P3O10) componente fundamental de los jabones, de detergentes y de productos diferentes para dulcificar las aguas duras. Usado también en alimentos. Tumorígeno en estudios en ratas.